- 首页 > 长链非编码 RNA 测序
长链非编码 RNA 测序
LncRNA高通量测序,采用去核糖体链特异性建库方法,对长链非编码 RNA、mRNA 、环状RNA等大RNA进行测序研究,从而快速全面准确地获得与特定生物学过程(例如发育、疾病等)所有大RNA转录本数据信息,可应用于细胞分化和发育的研究、调控机理的研究、疾病标志物的寻找、疾病的分子诊断、基因药物的研发等。
产品优势
1. 超高的技术稳定性
同一样本重复建库相关性Pearson值大于0.993;
2. 丰富的项目经验
已完成万例lncRNA项目,涉及人鼠及动植物物种;
3. 精湛的技术工艺
可承接人、鼠、动植物样品,外泌体、FFPE等,样品起始量低至20ng;
4. Dr.Tom多组学数据挖掘系统交付,分析无忧
一次测序即可获得mRNA、lncRNA、circRNA及关联数据分析结果;
10大数据库注释,多维度结果图片展示,数据图表循环挖掘;
ceRNA、蛋白、共表达、关键驱动基因互作网络分析可视化;
系统随时更新文献信息,查基因得文献,便于文章撰写;
5. 严格的质量管理
实验全程采用全方位质控体系,应用质量管理体系金标准;
6. 贴心的售后支持
7*24小时全天候技术支持,快速响应客户需求。
产品应用
1. 细胞分化和发育调控机理的研究
2. 疾病标志物的寻找
3. 疾病的分子诊断
4. 基因药物的研发
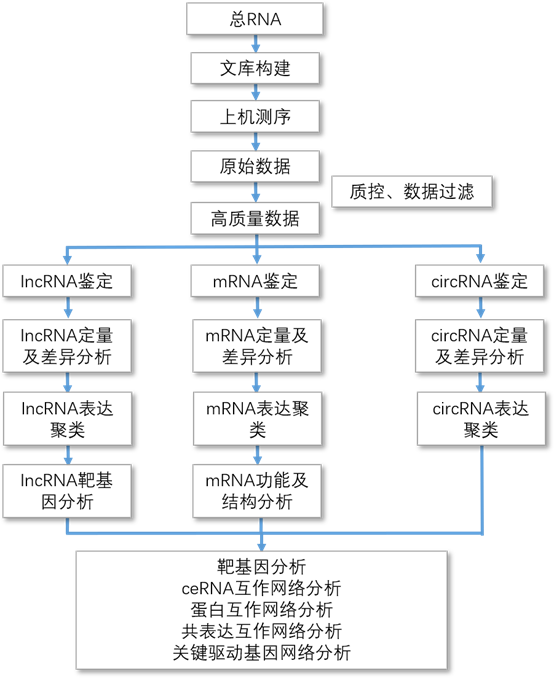
信息分析内容
标准信息分析(circRNA仅限人、小鼠)
1、基本数据统计
① 去除接头序列、低质量序列得到reads信息
② 样品相关性
③ 表达量分布
④ RNA分类
2、参考基因组比对
3、lncRNA、mRNA、circRNA鉴定
4、lncRNA、mRNA、circRNA定量分析
5、lncRNA、mRNA、circRNA差异表达分析(样本间、组间)
6、lncRNA、mRNA、circRNA表达/差异基因聚类
7、mRNA差异基因GO分类、富集
8、mRNA差异基因KEGG分类、富集
9、mRNA结构分析
① 可变剪切分析
② 融合基因分析(仅限人)
高级信息分析
一)数据库注释
1、转录因子注释(AnimalTFDB/PlantTFDB)
2、GSEA分析
3、Rfam、Pfam、Reactome、COG、EggNOG和InterPro数据库注释
二)互作网络分析
1、 靶基因分析
① miRNA-mRNA靶向关系分析
② lncRNA-mRNA靶向关系分析
2、 ceRNA互作网络分析
3、 蛋白互作网络分析
4、 共表达互作网络分析
三)特色分析
1、外部数据库关联分析(TCGA、ARCHS4)
2、关键驱动基因网络图分析
3、时间序列分析
lncRNA疾病标志物鉴定——CCR7趋化因子受体诱导的Inc-Dpf3通过抑制HIF1A-调节的糖酵解来抑制树突状细胞的迁移
Dendritic Cell Migration by Inhibiting HIF-1α-Mediated Glycolysis. Immunity. 2019 Mar 19;50(3):600-615.e15.
研究概要:
CCR7趋化因子受体刺激诱导快速但短暂的树突状细胞(DC)向引流淋巴结转移,这对于启动保护性免疫和维持免疫稳态至关重要。终止CCR7介导的DC迁移的机制仍不完全了解。本次研究发现了一个长链非编码RNA lnc-Dpf3,能够抑制CCR7介导的DC迁移。 在CCR7刺激下lnc-Dpf3的表达上调。DC特异的lnc-Dpf3的缺乏,导致CCR7介导的DC迁移增强,导致过度的适应性免疫反应和炎症性损伤。机制研究表明,CCR7刺激激活了DC中的HIF-1a转录因子途径,从而导致代谢重新编程为糖酵解以促进DC迁移。 lnc-Dpf3直接与HIF-1a结合并抑制糖酵解基因Ldha的HIF-1a依赖性转录,从而抑制DC糖酵解代谢和迁移能力。该研究证明了CCR7诱导型lnc-Dpf3在表观遗传和代谢途径与反馈控制DC迁移和炎症反应耦合中的关键作用。
研究策略:
研究样本:lnc-Dpf3 沉默和对照组的CCL19和CCL12刺激12小时的成熟的骨髓来源的树突细胞
研究技术:DNBSEQ 长链非编码RNA测序,免疫印记分析,流式分选,RT-PCR,RNA干扰
研究结果:
1. lnc-Dpf3抑制CCR7介导的DC迁移,lnc-Dpf3缺失导致CCR7介导的DC细胞迁移增强
通过lncRNA表达谱分析,在CCR7刺激的成熟的树突细胞中检测到34个差异lncRNA,对上调的18个lncRNA进行了qRT-PCR分析,发现其中6个在CCR7刺激后显著上调。对这6个lncRNA进行RNA干扰介导的功能筛选,研究人员发现了一条新长链非编码RNA lnc-Dpf3,并通过一系列功能学试验证明了该lncRNA在DC迁移调控中的作用。在趋化因子CCR7的刺激下,lnc-Dpf3的表达上升,并通过反馈性抑制下调了DC细胞向炎症部位的迁移。在DC条件性缺失lnc-Dpf3的小鼠中,CCR7所介导的DC细胞迁移增强,继而引发了更加严重的免疫炎症反应。
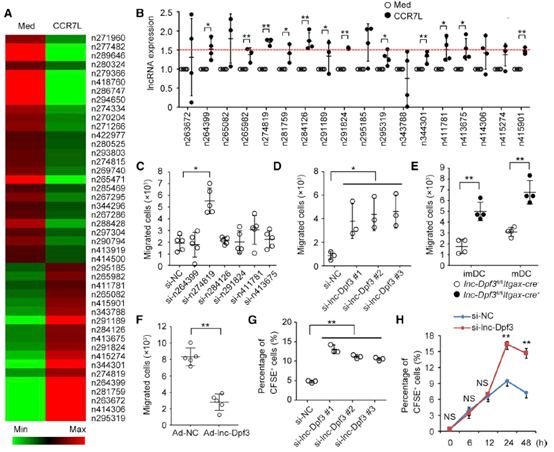
图1. lnc-Dpf3负调控CCR7依赖性树突状细胞迁移
2. lnc-Dpf3所参与的分子调控机制研究
在静息状态下的DC细胞中,转录后的lnc-Dpf3分子上带有m6A修饰。这些表观遗传学标记被Ythdf2蛋白特异性识别,进而引起lnc-Dpf3分子的降解;CCR7的刺激则会引起m6A的去甲基化,上调lnc-Dpf3在DC内的表达水平。进一步的转录组测序结果表明lnc-Dpf3与CCR7介导的转录因子HIF-1a活化息息相关。lnc-Dpf3的高水平表达抑制了HIF-1a引起的糖酵解,从而最终负向调控了树突状细胞的体内迁移。
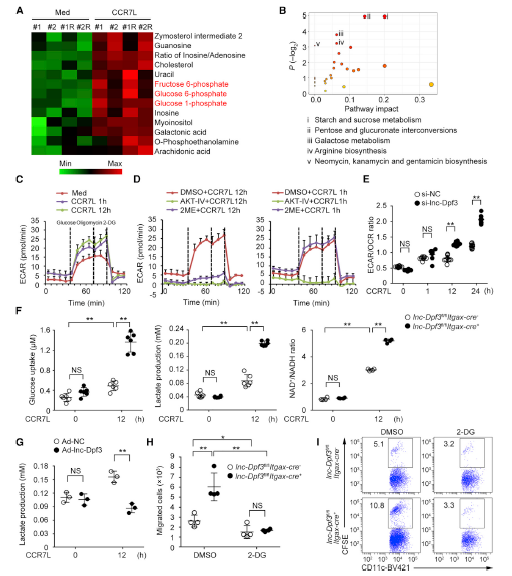
图2. lnc-Dpf3通过抑制hif -1a依赖的糖酵解来抑制DC迁移
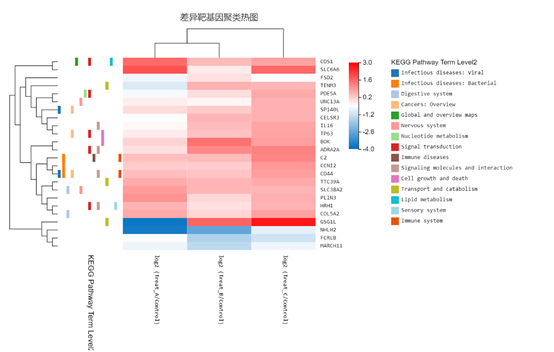
图1 lncRNA差异靶基因的聚类热图和KEGG功能富集图
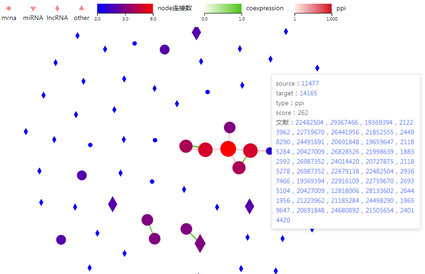
图2 差异表达lncRNA与靶基因的蛋白互作和共表达互作网络图
鼠标指连接线,可以立即展示相关文献信息
表1 lncRNA组织样品送样建议
组织类型 | 具体要求 |
新鲜培养细胞(细胞数) | ≥2×105 cell |
新鲜动物组织干重 | ≥30 mg |
全血 | ≥1 mL 全血收集的淋巴细胞 ≥1 mL Paxgene Blood RNA tube / RNAprotect® Animal Blood Tubes收集的全血 |
菌体(细胞数或干重) | ≥2×105 cell or ≥30 mg |
FFPE | ≥5片,未染色,100 mm2,5-10 μm厚度 |
表2 lncRNA测序样品判定标准
|
样本类型 |
总量 |
浓度 |
RIN |
28S/18S |
基线和 5S |
纯度 |
|
Total RNA |
≥200ng |
10-500 ng/μL |
RIN≥7.0 |
23S/16S≥1.0 |
基线平整,5S 峰正常 |
无 DNA,蛋白/盐离子等污染,样本无色透明不粘稠 |
|
Total RNA |
≥500ng |
40-1000 ng/μL |
RIN≥7.0 |
23S/16S≥1.0 |
||
|
FFPE RNA |
≥200ng |
70-500 ng/μL |
RIN≥2.0 |
DV200≥30% |
Q1:什么是长链非编码RNA?以及它们的作用?
哺乳动物基因组序列的约5%~10%被稳定转录,蛋白质编码基因仅约占1%,其余4%~9%的序列都转录为非编码RNA。而非编码RNA(non-coding RNA) 是指不能翻译为蛋白的功能性RNA分子。长链非编码RNA为这4%~9%中长度大于200nt的非编码RNA。它们的作用主要体现在四个方面:第一,影响周边基因的表达;第二,调控蛋白质活动及定位;第三,产生小分子RNA;第四,对其他RNA的调控作用[1]。
Q2:长链非编码RNA的建库方案是什么?
长链非编码RNA建库主要采用去除rRNA,构建链特异性文库,目前建库比较稳定。适用于人、鼠、动植物等物种。
Q3:长链非编码RNA主要签约风险有哪些?
rRNA去除效率不稳定,rRNA比例可能较高;只去除rRNA较适用于有良好参考基因组的项目,后续可以通过比对区分编码和非编码序列。
Q4:在信息分析中主要运用到的软件有哪些?
Tophat和Cufflinks(构建转录本),Infernal(家族分类),CPC(对转录本编码能力进行预测),Blast(比对),SOAP(过滤实验中未去除干净的rRNA,及lncRNA表达定量比对)。
Q5:长链非编码RNA建库测序结果可以用于分析环状RNA吗?
可以,长链非编码RNA建库模式采用去核糖体方式建库,对所获得的RNA进行打断测序,相当于获得全部RNA,即可以进行分析环状RNA表达情况,可应用于分析各物种环状RNA表达谱。
Q6:LncRNA测序数据中mRNA的定量效果如何?
人标品:已知mRNA定量与qPCR定量斯皮尔曼系数达到0.88。

