- 首页 > DIA蛋白定量
DIA蛋白定量
DIA 蛋白定量分析,主要采用数据非依赖性采集模式(data independent acquisition,DIA),通过液质联用技术(LC-MS/MS)对蛋白质酶解肽段进行质谱分析,结合传统的数据依赖性采集模式(data dependent acquisition,DDA)构建的谱图库,可对蛋白质组进行鉴定、定量,获得肽段、蛋白及所属物种来源、蛋白表达量变化等信息。
蛋白定量 DIA 目前主要在三种质谱仪器平台进行检测,常规 orbitrap 类仪器,timsTOF 类仪器以及更高分辨率的 orbitrap Astral 仪器等。
产品优势
- 国内唯一参与DIA测评及建立大队列DIA标准的企业,华大具有高水平的DIA技术交付能力,从鉴定数、重现性、线性、动态范围等方面看,已达到全球先进水平;具有极佳的软硬件优势和过硬的操作流程;
- 重复性、稳定性高达90%,是大队列血液样品蛋白质组研究首选技术;
- 针对富含临床信息的FFPE样品,提供低至1片的蛋白质组定量服务;
- 颠覆传统,创新性引入相关性差异分析,通过多维信息整合,稳健算法直击核心功能,精准锁定关键机制;
- 采用Dr. Tom云平台进行数据交付,便于开展零生信基础的数据挖掘,以及同转录组的自主关联分析;
- 提供经典的蛋白质组非靶向发现+靶向验证一站式服务;以及蛋白质组+转录组、蛋白质组+代谢组、常规蛋白质组+磷酸化蛋白质组学等一系列多组学关联分析服务;
- 提供配体-受体、激酶-底物及转录因子-靶蛋白等全方位分析,深入探索信号调控通路,更好地开展分子机制、生物标志物、疾病机理和药物开发研究(人、小鼠)。
产品应用
- 精准医疗领域
癌症研究:肿瘤组织个体差异大背景差异大,需要单个样本采样比较
个体医疗:大规模的数据采集,需要高稳定性和重现性的技术支撑
- 动植物微生物研究领域
环境适应性研究:多种环境不同水平的处理同时比较,需要高稳定性和重现性的技术支撑
模式生物机理研究:深入探究体内调控机理,实现不同组别差异蛋白比较
技术路线
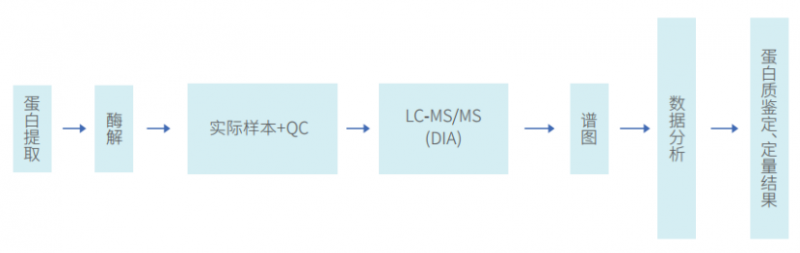
信息分析内容
信息分析条款 | 信息分析内容 |
标准信息分析 | 1 标准信息分析内容 1.1 数据产出统计 1.2 数据质控(组内变异系数、主成分分析以及样本定量相关性) 1.3 蛋白质鉴定和定量结果 1.4 蛋白质GO分析 1.5 蛋白质COG/KOG/eggNOG分析 1.6 蛋白质Pathway代谢通路分析 1.7 差异蛋白的GO富集分析 1.8 差异蛋白COG/KOG/eggNOG富集分析 1.9 差异蛋白的Pathway富集分析 1.10 重复性分析(仅针对设计了重复的实验) 1.11多样品间表达模式聚类(三个或三个以上样品可提供) 1.12 时间序列分析 1.13 差异表达蛋白互作分析 1.14 差异表达蛋白亚细胞定位 1.15 蛋白信号调控分析(针对人和小鼠) 配体-受体调控分析,激酶-底物调控分析,转录因子-靶蛋白调控,蛋白信号调控分析 |
1、肺腺癌化疗药物疗效生物标志物筛选
Identification of serum biomarkers to predict pemetrexed/platinum chemotherapy efficacy for advanced lung adenocarcinoma patients by data-independent acquisition (DIA) mass spectrometry analysis with parallel reaction monitoring (PRM) verification.
Translational lung cancer research. 2021
背景:
培美曲塞/铂化疗是肺腺癌患者的标准化疗方案,但疗效差异很大,寻找预测药物疗效的生物标志物至关重要。
实验设计:
接受培美曲塞/铂化疗的晚期肺腺癌患者的血清样本的DIA蛋白定量分析结合靶向蛋白质组学技术PRM验证。
主要结果:
1)发现阶段:选择20例接受培美曲塞/铂化疗的晚期肺腺癌患者的血清样本(其中12例疗效较好、8例疗效不佳),进行DIA蛋白定量分析,共发现23个显著差异表达蛋白(DEPs)。
2)验证阶段:采用靶向蛋白质组学技术PRM,对挑选的16个DEPs,分别在发现阶段的20例血清样本以及另外23例患者血清样本(16例疗效较好、6例疗效不佳)中进行验证。PRM的定量验证与DIA的结果有很好的相关性。
3)DIA发现+PRM验证的模式,发现谷胱甘肽过氧化物酶3 (GPX3)可作为潜在的生物标志物,这些生物标志物的潜在生物学机制有待进一步研究。

图1 GPX3的PRM验证结果
2、盐胁迫下玉米种子萌发的分子机制研究
Comprehensive transcriptome and proteome analyses reveal a novel sodium chloride responsive gene network in maize seed tissues during germination.
Plant, Cell & Environment. 2020
背景:
发芽是成熟种子的胚根穿透周围的屏障发育成幼苗的过程,已知多种环境因素会对其产生影响,但高盐环境如何影响玉米种子的发芽尚不清楚。
实验设计:
玉米种子分为SE盐处理胚胎组,SR盐处理胚乳组,CE胚胎对照组和CR胚乳对照组;每组3例生物学重复。利用SWATH(DIA)蛋白定量、RNA-Seq、qRT-PCR(验证)、靶向代谢组(检测脱落酸ABA的含量)等技术进行研究。
主要结果:
1)发芽试验表明,在200 mM NaCl处理下,离体胚能够萌发,而完整的种子受到高度抑制;推测玉米胚乳可能参与了盐信号对周围组织(如胚胎)的感知和转导,并表现出与拟南芥完全不同的反应。
2)盐胁迫反应一般会涉及ABA,通过分析体内ABA的分布和数量发现,与对照组相比,NaCl处理下离体胚的ABA水平没有增加,表明ABA水平的升高依赖于胚乳。
3)转录组和蛋白质组研究发现盐处理的胚胎和胚乳之间转录后和翻译后的变化存在显著差异,揭示了种子萌发在转录、转录后和翻译三个层面上的空间动态调控,进而提出了一种新的玉米种子盐胁迫感知和信号转导模型。
4)本研究采用的蛋白质组和转录组联合分析方法可用于寻找特定发育过程或应激反应主调控因子的相关研究。

图2 玉米种子盐胁迫感知和信号转导模型
1、蛋白鉴定和定量概况
表1 各样本鉴定结果概览
|
Name |
Peptide number |
Protein number |
|
N_1 |
73592 |
7123 |
|
N_2 |
83437 |
7720 |
|
…… |
…… |
…… |
表2 差异蛋白统计列表
|
Comparsion group |
Down-regulated |
Non-regulated |
Up-regulated |
|
T-VS-N |
381 |
8005 |
703 |
|
XR-VS-N |
242 |
8369 |
479 |
|
XR-VS-T |
137 |
9020 |
118 |


图1 差异蛋白统计图
以Fold change≥1.2和Q-Value<0.05两个条件作为显著性差异蛋白的筛选标准,得到组间上下调蛋白统计(左图)及火山图(右图)
2、质控



图2 质控结果
CV分布图(左图);主成分分析(PCA,中图);样本相关性分析热图(右图)
3、功能分析



图3 功能分析结果
GO功能注释(左图);pathway显著富集气泡图(中图);差异蛋白互作关系网络图(右图)
4、差异网络分析
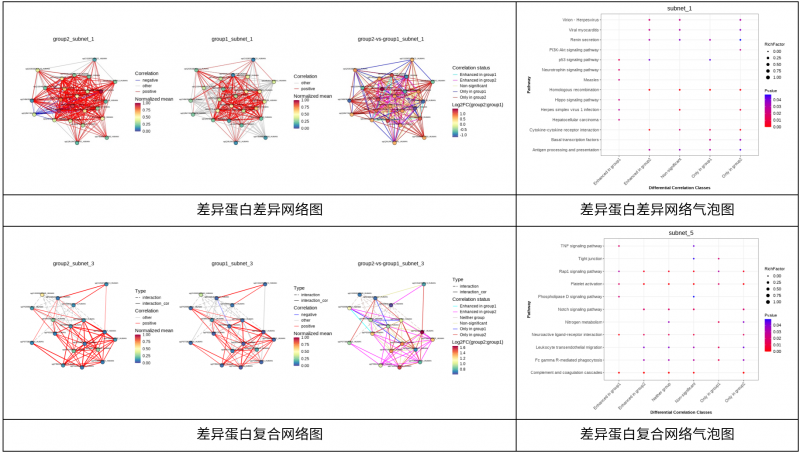
4、蛋白信息调控分析(针对人和小鼠)
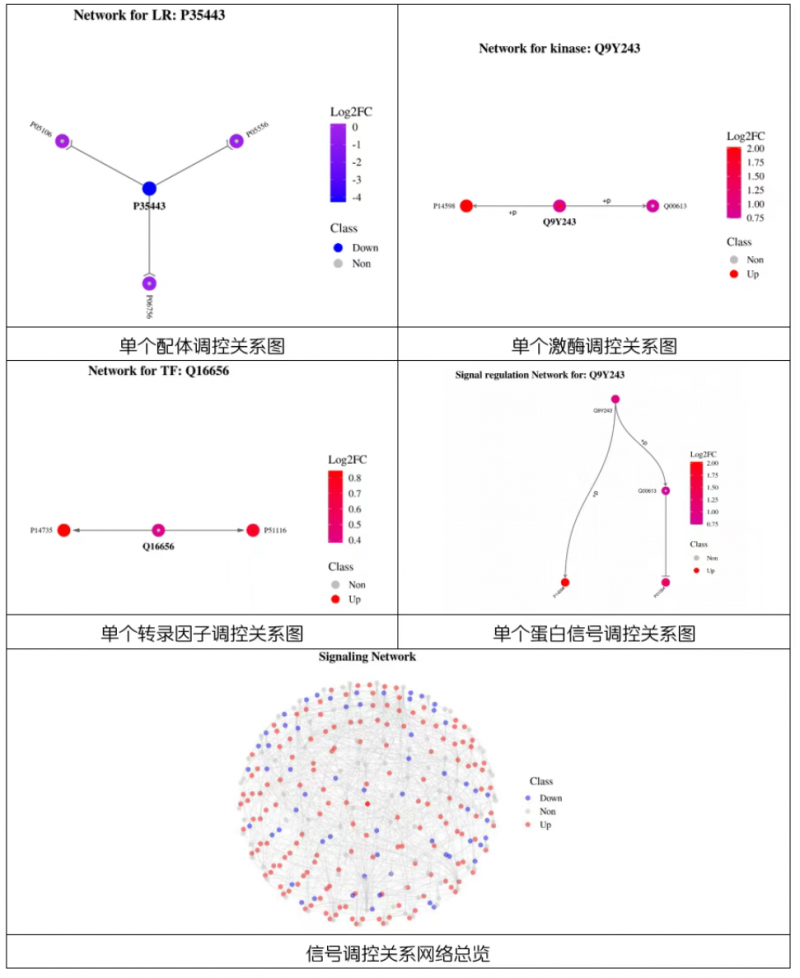
图4 部分分析结果示例
表1 组织类样品送样要求
样品类型 | 送样量 | 备注 |
新鲜动物组织干重 | ≥5mg | 富含杂质或蛋白质含量低的样品量干重≥5g,如植物的根、木质部、韧皮部组织等 |
植物和蕈类真菌(如蘑菇、木耳)类 样品量湿重 | ≥300mg | |
酵母、霉菌类真菌和细菌、噬菌体等微生物 | ≥50mg,或细胞数≥5×106 | |
新鲜培养细胞数(个) | ≥5×106(细胞沉淀体积约30μl~50μl左右) | |
客户分离好的外泌体 | ≥300μL,约1011Particles/mL | |
血液类(去高峰度) | 血清、血浆≥100µl | 解冻后血细胞会破裂,蛋白溶出来会影响分析,因此一般不建议送全血 |
表2 蛋白类样品送样要求
|
样本类型 |
送样量 |
|
蛋白液 |
≥40μg,浓度≥0.5µg/µL |
Q1:蛋白定量DIA和传统的非标记定量相比有何优势?
A1:传统的非标记定量一般需要通过分级的方法开展,耗时久、重复性差、数据结果可信度不高;蛋白定量DIA技术是新一代非标记定量技术,可通过更优的数据采集模式,在相同时间采集到更丰富的信息,压缩周期的同时,大福度提高样本间平行比较的重复性,数据结果可信度极高。

